Metainformationen zur Seite
Dies ist eine alte Version des Dokuments!
Das chemische Gleichgewicht
Statisches vs. chemisches Gleichgewicht
Du kennst das Wort „Gleichgewicht“ aus dem Alltag eher als statischen Zustand. Wenn man z.B. sich so auf einer Wippe positioniert, dass diese sich nicht mehr bewegt, befindet sich die Wippe im Gleichgewicht. Wenn du ruhig auf einem Balken stehst, befindest du dich im Gleichgewicht.
Bei chemischen Reaktionen gibt es ebenfalls Gleichgewichtszustände, die sich aber erheblich von dem Alltagserleben eines Gleichgewichtes unterscheiden. Man kann einfache Spiele durchführen, um die Natur eines chemischen Gleichgwewichts zu modellieren.
Modellversuch
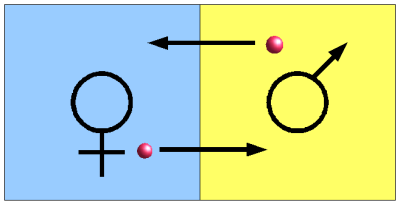
Eine Schulklasse wird in zwei Gruppen eingeteilt, z.B. Mädchen und Jungen. Alle müssen zur betreffenden Unterrichtsstunde einen Tennisball mitbringen. Danach benötigt man ein einfaches Spielfeld, wie es auf jedem Tartanplatz vorhanden ist, es reicht auch ein breiter Flur mit drei Linien:
Beide Gruppen dürfen gerne unterschiedlich groß oder „gut“ sein. Die Mädchen begeben sich in den einen Teil des Feldes, die Jungen in den anderen. Ziel ist es nun, die eigenen Tennisbälle in das Feld des Gegners zu rollen. Ankommende Bälle dürfen natürlich sofort wieder zurückgerollt werden. Das Werfen von Bällen ist verboten. Alle 15 Sekunden wird das Spiel unterbrochen und die Anzahl der Bälle für jedes Feld einzeln bestimmt. Dabei konnten z.B. folgende Werte ermittelt werden (16 Mädchen, neun Jungen):
| Zeit [s] | n(Bälle im Feld der Mädchen) | n(Bälle im Feld der Jungen |
|---|---|---|
| 15 | 10 | 15 |
| 30 | 11 | 14 |
| 45 | 8 | 17 |
| 60 | 10 | 15 |
| 75 | 7 | 18 |
| 90 | 12 | 13 |
| 105 | 11 | 14 |
| 120 | 9 | 16 |
| 135 | 13 | 12 |
| 150 | 8 | 17 |
| 165 | 5 | 20 |
| 180 | 11 | 14 |
| Mittelwerte: | 9,58 | 15,42 |
Erwartungsgemäß haben die Mädchen aufgrund ihrer Anzahl eine bessere Chance, ihr Feld „sauber“ zu halten. Wenn auch die Momentaufnahme durchaus unterschiedliche Verteilungen zeigen kann, pendelt sich in dem Zeitfenster t=180s eine konstante, gemittelte Verteilung ein - wenn man annimmt, dass sich während des Spiels die Spieltaktik nicht ändert.
Das ist umso erstaunlicher, als dass die SuS sich während des Spiel ständig bewegen und einsetzen müssen. Normalerweise denkt man bei einem Gleichgewicht ja eher an Ruhe und Entspannung. Auch die Verteilung der Bälle in beiden Feldern ist nicht gleichmäßig, sondern lediglich das Verteilungsverhältnis bleibt in einem Zeitraum Δt konstant.
Das Stickstoffdioxid/Distickstofftetraoxidgleichgewicht
Darstellung von Stickstoffdioxid aus Bleinitrat
Wird Bleinitrat erhitzt, zerfällt es in Blei(II)oxid, Stickstoffdioxid und Sauerstoff gemäß: $$2Pb(NO_3)_{2(s)} \longrightarrow 2PbO_{(s)} + 4NO_{2(g)} + O_{2(g)}$$
Darstellung von Stickstoffdioxid aus Kupfer und halbkonzentrierter Salpetersäure
Bei der Reaktion von halbkonzentrierter Salpetersäure mit Kupfer entstehen Kupfer(II)nitrat $Cu(NO_3)_{2(s)}$, Stickstoffmonoxid $NO_{(g)}$ und Wasser $H_{2}O_{(l)}$. Das Stickstoffmonoxid $NO_{(g)}$ reagiert mit Luftsauerstoff weiter zu Stickstoffdioxid $NO_{2(g)}$.
Halbkonzentrierte Salpetersäure ist eine saure Lösung bestehend aus Hydroniumionen $H_3O^{+}_{(aq)}$.
$$(1) \space \space HNO_{3(aq)} + H_{2}O_{(l)} \rightleftharpoons H_3O^{+}_{(aq)} + NO_{3(aq)}^{-}$$
Kupfer(II)nitrat ist ein Salz der Salpetersäure. Die römische Zwei im Namen (II) gibt einen Hinweis darauf, welche Ladung Kupfer nach der Reaktion trägt.
$$(2) \space \space Cu_{(s)} \rightleftharpoons Cu^{2+}_{(aq)} + 2e^-$$
Die Oxidationzahl des Kupfers erhöht sich, das Kupfer wird zum Kupfer(II)-Ion oxidiert. Damit handelt es sich um eine Redoxreaktion.
Als Reaktionspartner verbleiben noch Hydroniumionen und die Nitrationen, die die Elektronen des Kupfers aufnehmen müssen. Als Produkte müssen Stickstoffmonoxid und Wasser gebildet werden (solche Gleichungen werden im Abitur im Material i.d.R. gegeben):
$$(3) \space \space 4H_3O^{+}_{(aq)} + 3e^- + NO_{3(aq)}^{-} \rightleftharpoons NO_{(g)} + 6H_{2}O_{(l)}$$
Überschüssiger Sauerstoff reagiert sehr oft mit Hydroniumionen zu Wasser. Jetzt müssen zunächst Elektronen ausgeglichen werden (Gleichung (2) mit 3 multiplizieren und Gleichung (3) mit 2 multiplizieren),
$$(2a) \space \space 3Cu_{(s)} \rightleftharpoons 3Cu^{2+}_{(aq)} + 6e^-$$ $$(3a) \space \space 8H_3O^{+}_{(aq)} + 6e^- + 2NO_{3(aq)}^{-} \rightleftharpoons 2NO_{(g)} + 12H_{2}O_{(l)}$$
Jetzt muss in Gleichung (1) noch die Anzahl an Hydroniumionen angepasst werden (mit 8 multiplizieren):
$$(1a) \space \space 8HNO_{3(aq)} + 8H_{2}O_{(l)} \rightleftharpoons 8H_3O^{+}_{(aq)} + 8NO_{3(aq)}^{-}$$
Wenn man jetzt Hydroniumionen, Wassermoleküle und Elektronen kürzt, ergibt sich:
$$Gesamt: 3Cu_{(s)} + 8HNO_{3(aq)} \rightleftharpoons 3Cu^{2+}_{(aq)} + 2NO_{(g)} + 6NO_{3(aq)}^{-} + 4H_{2}O_{(l)} $$
Das Stickstoffmonoxid reagiert mit Luftsauerstoff zu Stickstoffdioxid:
$$2NO{(g)} + O_{2(g)} \rightleftharpoons 2NO_{2(g)}$$
Besonderheiten des Stickstoffdioxids
Stickstoffdioxid ist ein radikalisches Molekül:
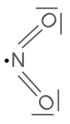
Es ist ein tiefbraunes Gas von chlorartigem Geruch. Du kannst vor allem im Winter in der Nähe von Dieselfahrzeugen seinen Geruch wahrnehmen, wenn deren Motor noch nicht warmgefahren ist, sodass die Stickoxide noch nicht vom Katalysator neutralisiert werden können.
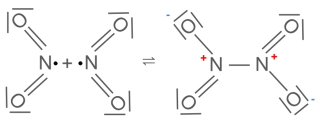
Da Radikale sehr instabile Verbindungen sind mit dem Bestreben unter Verlust ihrer radikalischen Eigenschaften zu reagieren, verbinden sich einige Moleküle des Stickstoffdioxids zu farblosem Distickstofftetraoxid.
$$N_{2}O_{4(g)} \rightleftharpoons 2NO_{2(g)} ; \Delta H_{r}^{0} = 57 \frac{kJ}{mol} $$
Formulierung als Gleichgewicht
Da es sich um Gase handelt, lassen sich Konzentrationen nicht angeben. Man weicht auf den Partialdruck p aus.
$$K_p = \frac{p(NO_{2(g)})^2}{p(N_{2}O_{4(g)})} $$
Prinzip von Le Chatelier
„Übt man auf ein chemisches System im Gleichgewicht einen Zwang aus, so reagiert es so, dass die Wirkung des Zwanges minimal wird.“